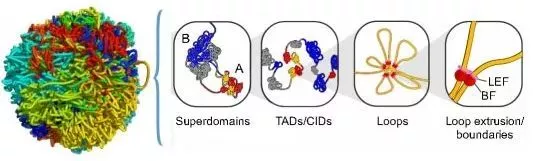
关于Hi-C
Hi-C(High-through chromosome conformation capture)技术源于染色体构象捕获 (Chromosome conformation capture, 3C)技术,以整个细胞核为研究对象,利用高通量测序技术,结合生物信息分析方法,研究全基因组范围内整个染色质DNA在空间位置上的关系,通过对染色质内全部DNA相互作用模式进行捕获,获得高分辨率的染色质三维结构信息。
(引自Pueschel R, Coraggio F, et al. From single genes to entire genomes: the search for a function of nuclear organization. Development , 2016 , 143 (6) :910)
通过Hi-C技术可以获得全基因组范围内的互作信息,得到染色体三个层级的三维结构:A/B compartment、拓扑相关结构域(TAD)、染色质环(loop)。
解析文献
Alterations in promoter interaction landscape and transcriptional network underlying metabolic adaptation to diet
期刊:Nature Communications
IF:11.878
背景
为应对可能对健康产生重大影响的食物供应和食物营养含量的波动,动物对营养质量和有效性的响应范围已经进化到从完全缺乏营养素到过量。随着西方生活方式的普及,高脂肪、高能量饮食,肥胖和NAFLD成为人们日益关注的健康问题。在卡路里过多的情况下,肝脏通过动态转录组重编辑来适应营养过剩,这是维持代谢体内平衡所必需的多种适应之一。目前基因调控对介导肝脏代谢适应过多卡路里摄入的机制未完全了解,对启动子-增强子互作动力学的详细分析,可以了解从营养诱导的代谢适应到疾病发展的过程。增强子通常距离其靶基因很远,因此难以准确地研究将特定的增强子分配给其靶基因及基因调控的细节。Hi-C被应用于识别全基因组染色质相互作用,并提供对高阶染色质组织的了解。
作者采用饮食诱导肥胖的C57BL / 6J小鼠模型,在这些小鼠的肝脏组织上进行了Hi-C和PCHi-C,结合ChIP-seq和RNA-seq,以研究饮食诱发肥胖过程中启动子锚定的染色质互作动力学。
结果
1、慢性肥胖致肝脏转录组重编
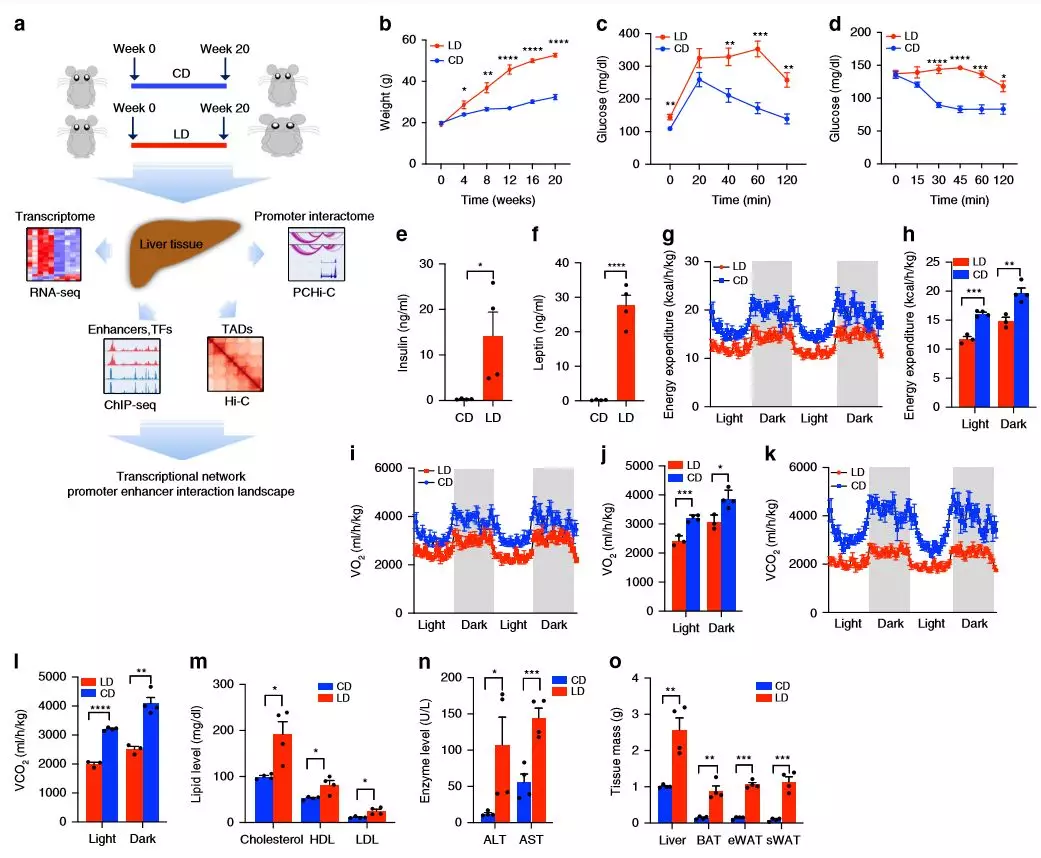
作者对雄性C57BL / 6小鼠进行了饮食研究,五周大的小鼠适应普通饮食(NIH-31),随后(每组5只小鼠)接受高碳水化合物和高脂的饮食20周。在研究过程中,高脂饮食的小鼠明显肥胖,在20周后总体重几乎是高碳水化合物饮食的两倍。肥胖小鼠的葡萄糖和胰岛素耐受性较差,血浆胰岛素和瘦蛋白水平显着增加,这表明它们的代谢功能异常。
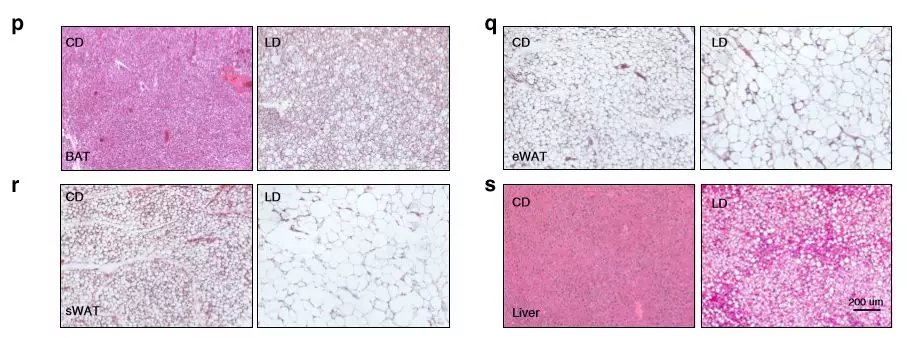
为了确定肥胖如何影响全身代谢,将喂食LD(高碳水化合物饮食)和CD(高脂饮食)的小鼠测量其耗氧量(VO 2),二氧化碳产生量(VCO 2)和能量消耗(EE)。与CD组相比,LD组的平均EE,VO 2和VCO 2值降低,血浆总胆固醇,高密度脂蛋白(HDL),低密度脂蛋白(LDL),天冬氨酸转氨酶(AST)和丙氨酸转氨酶(ALT)明显升高。LD组脂肪组织和肝脏质量均显著高于CD组,脂肪细胞大小增加。
图1饮食对代谢参数的影响
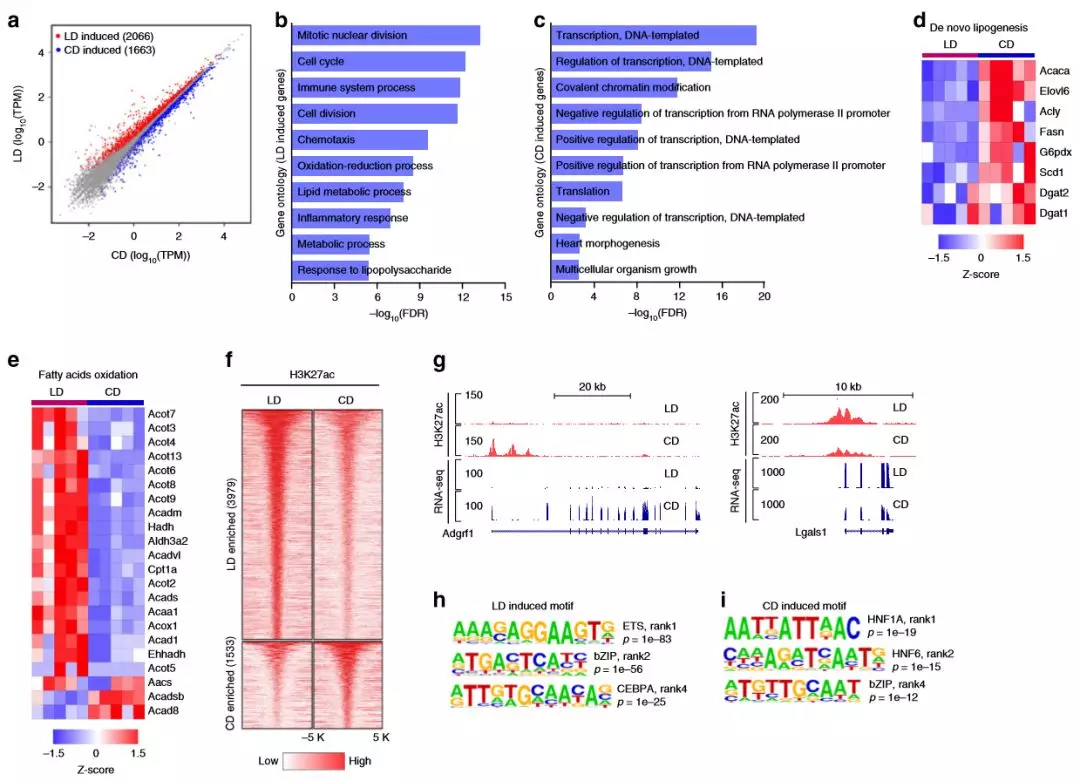
为了解肥胖的转录反应,作者对研究小鼠(每组5只)的肝脏进行RNA-seq,差异表达基因(DEG)分析确定了高脂肪饮食的肥胖组中有2066个基因上调,而高碳水化合物饮食组有1663个基因上调。在慢性肥胖和NAFLD中,脂质代谢受到干扰,其特征是介导新脂质生成(DNL)的基因下调,而涉及脂肪酸氧化的基因(FAO)上调。转录组中的差异反映了高脂质和高碳水化合物的饮食在小鼠肝脏中活跃的代谢状态和调控网络的差异。
2、慢性肥胖改变了肝脏的增强子网络
为了解适应肥胖是如何影响增强子活性,作者通过肝脏组织ChIP-seq对H3K27ac(每组3只)进行了分析。研究发现差异富集的基因座大多位于远离TSS的位置,并且被归类为增强子。高脂饮食组中富含H3K27ac的区域,最富集的基序对应于ETS(ETS1,EHF),bZIP(FOSL2,JUN-AP1和ATF3)和C / EBP(C / EBPA, C / EBPB和C / EBPE)家族转录因子。
图2慢性肥胖的肝脏转录组和增强子网络会重编辑
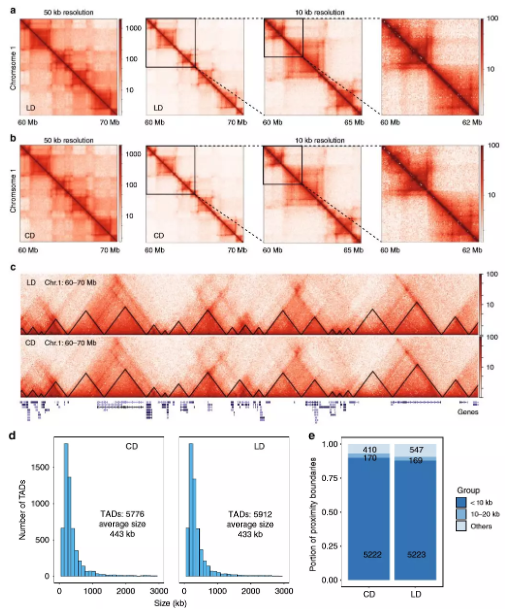
3、肥胖不会改变与拓扑相关结构域
为详细了解染色质互作,作者在高碳水化合物和脂质的饮食中对小鼠(每组2只)的肝脏进行了原位Hi-C处理。与预期一样,饮食和肥胖及其所有相关的生理和代谢变化均未影响A和B区室的模式。作者比较了两组之间的TAD边界,约90%的边界相同,表明在肥胖和NAFLD期间高阶染色质组织保持不变。
图3慢性肥胖肝脏中的高级染色质结构
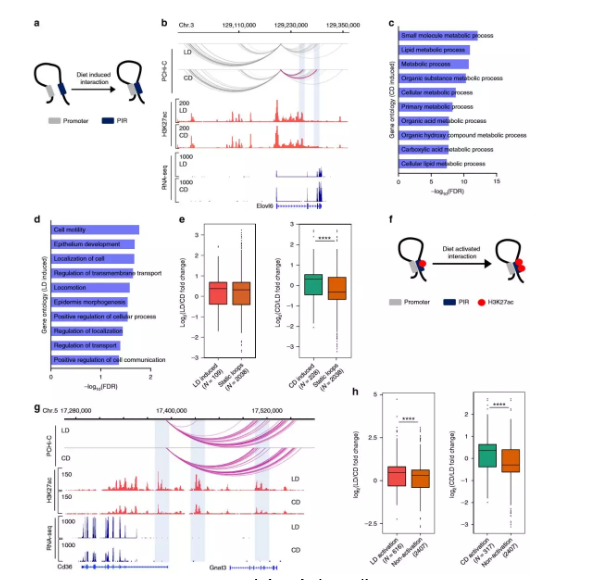
4、在代谢适应中促进染色质相互作用
作者在Hi-C数据中发现高脂质饮食的肝脏中34,982个显着的染色质互作,以及高碳水化合物饮食中37,185个显着的染色质互作,分别有28,682和30,502个染色质相互作用与基因启动子(TSS +/- 2 kb)重叠。为获得肝脏中启动子锚定的染色质互作及其在适应肥胖后的变化的高分辨率视图,作者进行了启动子捕获Hi-C(PCHi-C)(每组2只)。LD和CD组共享了很大一部分交互作用(54%),这表明许多启动子互作是稳定的。几乎80%的相互作用跨越<500 kb,大约13%的相互作用发生在两个启动子之间,表明启动子调控远端基因元件。
为了解启动子相互作用对基因表达的潜在调控作用,作者将启动子互作与基因表达相关联。通常,启动子互作的数量增加与基因表达呈正相关,作者还观察到也富集了未表达基因的启动子互作,这表明某些启动子相互作用是预先形成的,而不是由增强子激活诱导的。作者测试了H3K27ac富集与启动子互作区域(PIR)的交集,值得注意的是,具有H3K27ac富集的PIR与基因表达的增加显著相关,这支持启动子与活性增强子的接触会上调基因表达的模型。
图4在代谢适应饮食中启动子锚定的染色质互作调节的基因表达变化
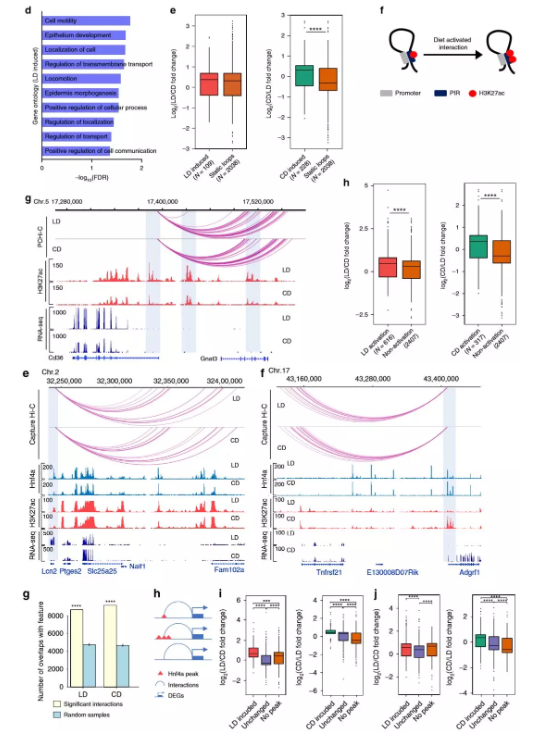
5、差异表达基因的启动子接触改变
为了解代谢适应饮食是否改变了肝脏中的启动子环化,作者使用了edgeR 来鉴定染色质相互作用模式的差异。其中1962个重编的启动子相互作用中,高脂质的饮食中增加705次,而高碳水化合物的组中增加1257次,分别与109和228 个DEG重叠。比较与静态环相关的DEG,只有对高碳水化合物的饮食有反应的启动子/增强子相互作用与基因表达的增加显着相关。这表明,新形成的启动子互作有助于代谢基因的转录调控,并且可能与饮食有关。
6、预形成的启动子-增强子相互作用
为了解在Hi-C数据中,与启动子互作的增强子的活性状态是否反映了基因表达,作者检查了差异富集的H3K27ac与启动子远端互作位置的重叠,发现了4449个启动子-增强子相互作用,其中H3K27ac在高脂质的饮食组中差异性富集。无论饮食如何,启动子与乙酰化增强子互作的DEG均上调,在预形成的环中,增强子的激活状态发生变化的启动子-增强子环的数量(6452)大大超过了条件变化后形成的新环的数量(1962)。这些发现表明,已经与启动子互作的增强子的激活,代表了代谢应激期间远端基因调控的一种重要模式。
图5 饮食改变了启动子互作
7、转录组分析将Hnf4α与代谢联系起来
为了评估哪些转录因子结合参与基因表达变化,作者在启动子中进行了基序分析,观察到包括Hnf4α 的几个TF基序的富集 ,HNF4α是信号响应转录因子,在调节脂质代谢中起重要作用。作者通过qPCR和免疫印迹,发现肥胖组中Hnf4α在蛋白质和mRNA水平上的下调,C18多不饱和脂肪酸包括亚油酸是HNF4α的已知配体。接下来,作者进行了ChIP-seq(每组2只),以了解Hnf4α如何响应肥胖。肥胖组中更多的Hnf4α富集峰与脂质配体对Hnf4α的活化相一致,作者还观察到启动子的远端互作与Hnf4α结合重叠,这表明Hnf4α与启动子互作的位点结合。启动子远端互作位点Hnf4α峰增加,DEGs也显示基因表达上调。
图6 转录组分析将Hnf4α与NAFLD的代谢基因的调节联系起来
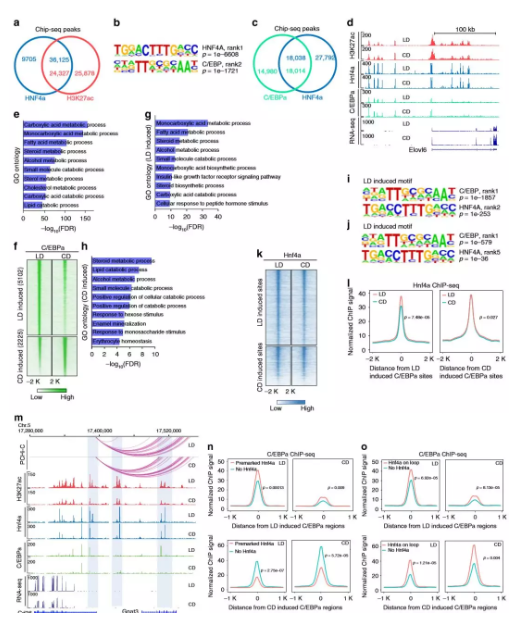
8、Hnf4α与其他转录因子结合
尽管作者确定了大约4000个发生了变化的Hnf4α结合位点,但这个数字仅代表约10%的Hnf4α的全基因组结合位点。在所有Hnf4α结合位点中,有79%与富集H3K27ac的基因座共定位,这表明肝脏中大多数已鉴定的Hnf4α结合区域是在两种情况下都存在且活性元件或开放染色质不易改变。如此大比例的Hnf4α结合位点是稳定的,作者假设Hnf4α可能在代谢应激期间与其他转录因子发生功能性相互作用,研究了Hnf4α结合的激活区域中存在哪些转录因子结合基序,最显着富集的共有基序是HNF4α,第二个转录因子是基本亮氨酸拉链结构域(bZIP)家族,其中包括C / EBP家族。
为了验证基序结果,作者进行了C /EBPαChIP-seq(每组2只),发现在肝脏中有55%的C /EBPα峰与Hnf4α共定位,共结合位点涉及多种代谢途径的基因,包括羧酸代谢,脂肪酸代谢,类固醇代谢和脂质分解代谢。作者在C /EBPα差异结合位点检查了Hnf4α结合信号,Hnf4α信号在差异富集的C /EBPα区域较高,表明至少在这些位点上始终存在Hnf4α。这些数据表明,在与饮食的代谢适应过程中,Hnf4α经常与C /EBPα结合以调节基因表达。
图7 Hnf4α经常与C /EBPα共结合
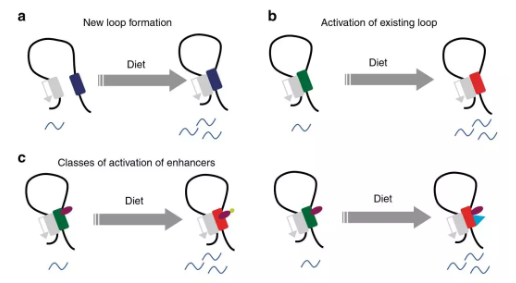
图8代谢适应饮食的启动子/增强子互作
总结
代谢适应营养状态需要改变关键组织中的基因表达。作者研究了染色质相互作用动力学,以及在小鼠模型系统中顺式调控基因座和转录网络的变化。与高碳水化合物的饮食相比,长期摄入高脂肪的饮食会导致肝脏转录网络发生严重的重编。通过启动子捕获Hi-C技术发现,启动子与远端调节基因座的远距离相互作用受代谢状态的调节,而代谢状态具体取决于饮食。对高脂饮食的适应主要由包括Hnf4α在内的受体介导,这适应取决于增强子/启动子环激活。适应富含碳水化合物的饮食,导致预先形成环的活化和新形成的启动子/增强子互作。这些结果表明,对营养变化和代谢应激的适应性是通过从头和已有的染色质互作而发生的,它们对代谢信号的反应不同。
画重点
公众号:金开瑞生物,对话框回复:饮食诱发肥胖
即可获得全文PDF
关于我们
武汉金开瑞生物工程有限公司提供的DLO Hi-C技术,是一种创新的染色质构象捕获技术,此技术信噪比高,质量控制于早期,为解析基因组三维结构提供了一种新型、高效、经济的研究方案。
技术优势
1.微量细胞建库:正常建match库与生信分析的样本量可低至10万个核。
2.高成功率:细胞样本文库构建成功率几乎为100%。
3.建库周期短:只需执行两轮简单的消化和连接步骤即可获得高质量的文库。
4.数据更准确:测序前质检,确保数据准确性
5.分辨率更高:在测序数据量更少的情况下,互作矩阵分辨率更高,染色质结构分析得到的数据也更多
6. 较高的信噪比:使用多种措施来减少噪音,保证高质量的数据输出,分析更准确。
7. 量身定制个性化分析方案:提供DLO Hi-C的标准分析外,更注重与RNA-Seq、ChIP-Seq、ATAC-Seq和甲基化等多组学表观遗传分析,提供个性化的生信分析方案。